
|
Читайте также: |
Влияние концентрации на скорость реакций определяется законом действующих масс. Закон Гольдберга и Воаге: при постоянной температуре скорость химической реакции прямо пропорциональна произведению концентраций реагирующих веществ, взятых в степенях их стехиометрических коэффициентов.
аА + вВ ↔ сС + dD
V = k*[A]a + [B]b
[A] и [B] – молярные концентрации реагентов
а, в – степени концентрации, равные стехиометрическим коэффициентам, только для простых реакций
в случае многостадийных реакций: V = k*[A]na + [B]nb
na, nb – постоянные, не зависящие от концентрации числа, называемые показателями порядка реакций по реагентам А,В определяются экспериментально, имеют значение от 0 до 2.
Порядок реакции. Реакции первого, второго, нулевого порядка. Физический смысл константы скорости реакции. Молекулярность элементарного акта реакции. Условия несовпадения порядка и молекулярности реакции. Вывод кинетического уравнения для реакции первого порядка. Время полураспада для реакций первого порядка.
Порядок реакции – показатель степени концентрации реагирующего вещества в кинетическом уравнении реакции.
Общий порядок химической реакции – величина равная сумме показателей степени концентрации реагентов в кинетическом уравнении реакции.
n = na + nb
k – константа скорости реакции, показывает какая доля из общего числа в расчете на один моль вещества приводит к химическому взаимодействию; зависит от природы реагирующих веществ, температуры среды, налия катализатора, но не зависит от концентрации реагирующих веществ.
Существуют реакции нулевого порядка: скорость =const
Существуют реакции I, II и III порядка.
Реакции нулевого порядка протекают с постоянной скоростью и не зависят от концентрации реагирующих веществ.
Для многостадийных процессов порядок реакции определяется самой медленной(лимитирующей) стадией.
Если вещество взято в избытке, то оно не участвует в определении порядка реакции, т.к. его концентрация практически не меняется.
Молекулярность – число молей веществ, участвующих в элементарном акте взаимодействия.
· Мономолекулярные
· Бимолекулярные
· Тримолекулярные – очень редки, т.к. одновременное столкновение трех молекул маловероятны
Порядок и молекулярность совпадают только для простых реакций.
Знание порядка реакции необходимо т.к. по нему определяется кинетическое уравнение для расчета константы скорости реакции.
Вывод кинетического уравнения I порядка:
А  В
В
t₀ = 0, [А] = С₀ - x, [В] = 0 - исходная концентрация
ч/з t: [А] = С₀ - x, [В] = x - прореагировало
V = k₁ * [С₀ - x]
 = k₁* [С₀ - x]
= k₁* [С₀ - x]  = k₁*
= k₁* 
 =
= 
-  = k₁ * t + I, I = -
= k₁ * t + I, I = -  , -
, -  = k₁ * t -
= k₁ * t - 
 = k₁ * t, k₁ =
= k₁ * t, k₁ =  *
*  ,
, 
k₁ =  *
*  [k
[k  = с-1, мин-1, час-1
= с-1, мин-1, час-1
в кинетике часто пользуются понятием полураспада реакции – время необходимое для того, чтобы прореагировала половина исходного количества вещества.
 ½ =
½ =  *
* 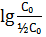 =
=  *
*  =
=  =
= 
Период полураспада реакции первого порядка не зависит от концентрации.
Дата добавления: 2015-07-11; просмотров: 278 | Нарушение авторских прав
| <== предыдущая страница | | | следующая страница ==> |
| Нарушение кислотно-щелочного равновесия. Ацидоз, алкалоз. Способы их устранения. | | | Зависимость скорости реакции от температуры. Правило Вант-Гоффа. |